【摘要】 从化工热力学角度出发,讨论当前工业生产常用的氧气氧化法制环氧乙烷工艺中,乙烯氧化反应单元氧化反应器易发生“飞温”,而导致火灾爆炸等重大事故的原因:主副反应均为放热反应;副反应为完全氧化反应,反应热为主反应的十几倍;温度升高将导致反应选择性下降,速率加快,系统进入“自热”状况,进而导致热失控,甚至引发火灾爆炸事故。进而提出温度控制是保证氧气氧化法制环氧乙烷生产安全的关键,并建议工业生产中采用改善反应器结构、改良催化剂、改进换热方式、加入抑制剂以及采用比热容更大的甲烷气致稳等控温措施。
【关键词】 环氧乙烷;氧气氧化法;热力学;列管式反应器;爆炸机理
0 引言
环氧乙烷(EO),分子式C2H4O,为第2.1类易燃气体,常温常压下为无色气体,低温时为无色透明液体,易挥发,闪点低于17.8℃,其蒸气能与空气形成范围广阔的爆炸性混合物,爆炸极限为3.0%~100%。遇热源和明火有燃烧爆炸的危险。若遇高热可发生剧烈分解,引起容器破裂或爆炸事故。接触碱金属、氢氧化物或高活性催化剂如铁、锡和铝的无水氯化物及铁和铝的氧化物可大量放热,并可能引起爆炸。其蒸气比空气重,能在较低处扩散到相当远的地方,遇火源会着火回燃。
环氧乙烷是石油化学工业的重要原料,除主要用于生产乙二醇外,还大量用于生产非离子表面活性剂、乙二醇醚等多种化工产品;在医药上广泛用作气体灭菌剂,在常温下能杀灭一切病原体。在乙烯的系列产品中,其产量仅次于聚乙烯,且具有很大的潜在市场。环氧乙烷的工业生产方法有氯醇法和直接氧化法,1960年以后,氧气氧化法由于乙烯消耗定额低,且廉价纯氧易得等因素,已成为环氧乙烷生产的主要方法[1]。
用氧气氧化法制环氧乙烷,氧化反应为强放热反应,正常情况下系统处于热平衡状态[2]。若由于反应条件的变化破坏了系统的热平衡,导致放热速率大于散热速率,系统温度将不断升高,而由于反应速率对温度变化非常敏感,温度升高会促使反应速率加快,系统将进入“自热”。一旦温度达到临界点,系统会出现热失控,甚至爆炸[2]。
笔者从热力学角度出发,讨论工业上乙烯氧化制环氧乙烷反应过程中氧化反应器易发生“飞温”导致火灾爆炸等重大事故发生的原因,进而提出当前工业中环氧乙烷氧化反应参数控制中应注意的问题。
1 乙烯氧化反应工艺流程分析
1.1 氧气氧化法生产环氧乙烷总工艺流程
氧气氧化法制环氧乙烷工艺流程如图1所示,包括乙烯氧化反应和吸收,CO2脱除,EO回收,EO精制4个单元。
图1 氧气氧化法制环氧乙烷工艺流程图
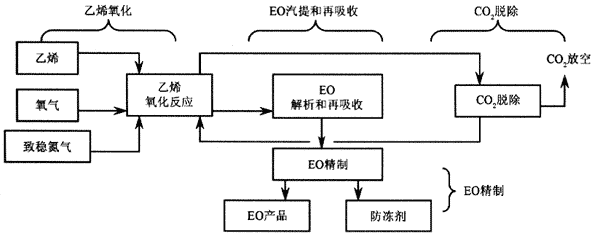
1.2 乙烯氧化单元工艺流程分析
氧化反应单元中,氧气和乙烯通入反应循环气,在氮气致稳下,以二氯乙烷为抑制气,预热后在催化剂床层进行催化氧化反应。
工业生产中,银催化剂是生产环氧乙烷惟一有效的催化剂[4-5],国内外相关文献报导很多[6-7]。由于细颗粒的银催化剂易结块、磨损,催化质量容易恶化,导致催化剂效率急速下降等原因,工业生产中普遍采用列管式固定床反应器(见图2)。
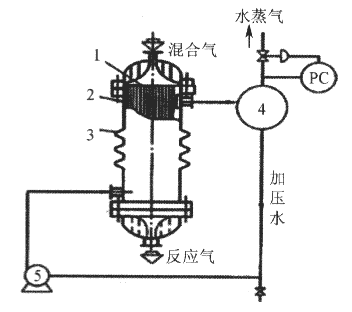
图2 列管式固定床反应器
1-列管上花板;2-反应列管;3-膨胀圈;4-气水分离器;5-加压热水泵;PC-控制系统
2 反应过程的热力学分析
2.1 氧化单元反应过程
乙烯氧化合成环氧乙烷是个串、并联共存的反应网络,其反应过程可以用以下网络反应方程式表示:
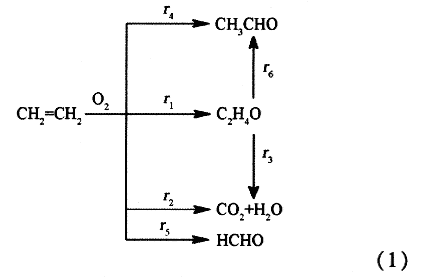
则生成环氧乙烷的选择性可以表示为
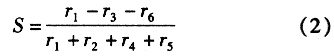
工业生产中,在银催化剂的作用下,反应产物里实际上主要是环氧乙烷、二氧化碳、水,而甲醛、乙醛的量非常少,因此,r4,r5,r6可以忽略不计,即可简化为

则主要的反应网络可表示为

2.2 氧化单元热力学分析
由热力学知识[8]可知,通过计算反应过程的焓变和自由焓变可以确定在一定条件下反应进行的方向以及能量发生的变化。反应过程焓变和自由焓变可由下式求得:
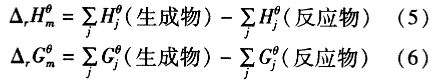
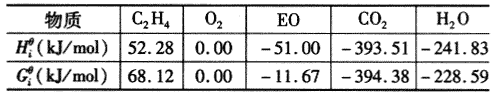
各反应物及生成物的热力学数据[9-10]如表1所示,标准状态下各主要反应的热力学状态函数如表2所示。可以看出,主要副反应过程放出的反应热![]() 是主反应 的十几倍。由
是主反应 的十几倍。由![]() 可知上述各反应均为自发进行的化学反应。
可知上述各反应均为自发进行的化学反应。
表1 各种气体标准热力学数据
2.3 温度对主副反应的影响
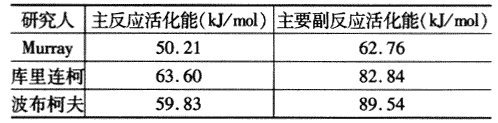
在乙烯环氧化过程中主要的外界因素是反应温度。氧化法制环氧乙烷均采用银催化剂,关于银催化剂上主反应和主要副反应的活化能前人已经用不同的催化剂进行过测定,其数据如表3所示。由表中可以看出,尽管各研究者所测得数值略有差异,但环氧化反应活化能(E1)小于完全氧化副反应的活化能(E2)这一定性结论是一致的。
表3 在银催化剂上主、副反应的活化能
由化学动力学理论[9]可知,化学反应速率随温度变化如下:
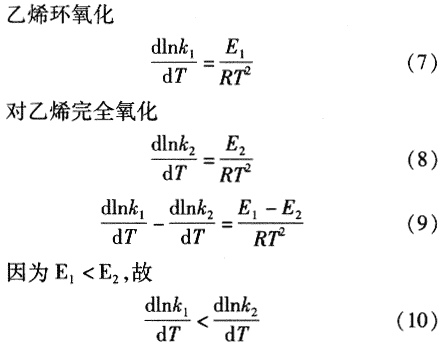
对于平行反应,如果主反应活化能大于副反应活化能,温度增高有利于选择性的增大;反之,降低温度有利于选择性的增大。由上述推导可知:随着反应温度的升高,两个反应速率都在增加。乙烯完全氧化反应速率随温度增加快于乙烯环氧化反应。
由上分析,乙烯氧化制环氧乙烷主副反应均为强放热反应,温度对反应的选择性较为敏感,对于这种反应最好采用流化床反应器。由于所使用催化剂原因选用了固定床反应器,该类反应器的显著缺点就是:传热效果差。乙烯氧化反应过程中,反应器径向和轴向都存在温差。列管式固定床反应器的温度分布如图3所示。沿轴向温度分布有一个最高温度,称为热点。热点以前放热速率大于散热速率,热点以后则相反。热点温度过高,会使反应选择性降低,催化剂作用变慢,甚至使反应失去稳定性或产生飞温,导致火灾爆炸事故。
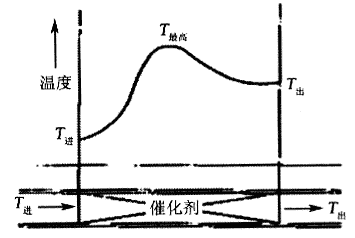
图3 列管式固定床反应器的温度分布
T进-反应器进口温度;T出-反应器出口温度;T最高-热点温度
由式(8)~式(10)推导知,随着温度提高,主、副反应速率同时加快,副反应速率提高快于主反应,选择性下降。由表2数据知,完全氧化反应的促进将导致放出更多的热量,使温度进一步升高,如果不能及时移走反应发出的大量的热量,导致催化剂床层“飞温”,则可能导致热爆炸事故的发生[11]。
3 工业生产中建议采取的控温措施
3.1 反应器结构的改进
可通过扩大反应管的直径、减少反应管根数或串联多个反应器的方法减弱反应状态的差异,降低局部飞温发生的可能性。
3.2 催化剂的改进
可通过在原料气中带入微量抑制剂,使催化剂部分毒化,降低催化性能;在原料气入口附近反应管上层放一定高度的惰性载体稀催化剂,或放一定高度已部分老化催化剂,降低人口附近反应速率以降低放热速率;选用传热性能好的环形载体催化剂,环形可克服球形载体催化剂气体走短路的缺点,气体搅动激烈,传质传热速率快,有利于热量的移出。
3.3 换热方式的改善
增大换热面积及合理选择载热体以增大换热系数。一般反应温度在240℃以下宜采用加压热水作载热体。反应温度在250~300℃可采用挥发性低的矿物油或联苯醚混合物等有机载热体。反应温度在300℃以上则需用熔盐作载热体。
分享按钮责任编辑 :老芋头 (易 安 网 版 权 所 有 ,未 经 授 权 禁 止 使 用 ,不 能 转 载 ! )
2013 ©易安网. ALL Rights Reserved. 京ICP备11028188号 | 京公网安备11010502022994